表的内容
补体的激活涉及蛋白质的顺序蛋白水解,产生具有蛋白水解活性的酶复合物。蛋白水解级联反应允许巨大的放大,因为每一步激活的酶分子可以在下一步产生多个激活的酶分子。补体活化的产物以共价附着在微生物细胞表面,附着在与微生物和其他抗原结合的抗体上,以及附着在凋亡小体上。补体激活被调节蛋白抑制,这些调节蛋白存在于正常的宿主细胞中,而不存在于微生物中。调节蛋白是对正常细胞的适应,使得对宿主细胞的补蛋白损害最小化。微生物缺乏这些调节蛋白,其允许在微生物表面上进行补体激活。
图像来源:创意诊断
补充激活通过以下三种途径中的任何一种:
- 经典的途径
- 另一种途径
- 章节途径
补体系统被微生物和附着在微生物和其他抗原上的抗体激活。
古典途径
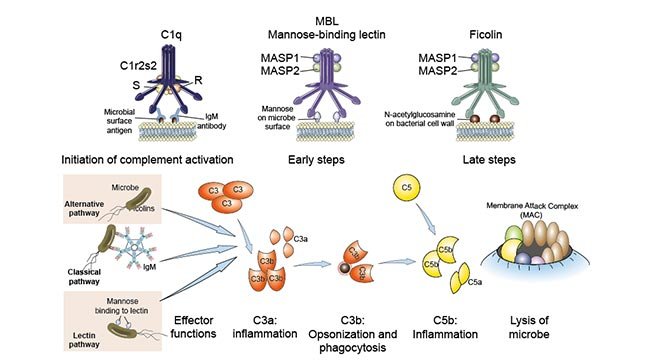
它是由与抗原结合的某些同类型抗体激活的;的替代路线,在没有抗体的情况下在微生物细胞表面被激活;和凝集素途径,由血浆凝集素激活,血浆凝集素与微生物上的甘露糖残基结合。尽管补体激活的途径在启动它们的情况下不同,但所有这些都导致生成能够切割最丰富的补体蛋白C3的酶络合物。经典的通路,所谓的,因为它首先被发现,使用称为C1Q的血浆蛋白检测与微生物或其他结构的表面结合的抗体。一旦C1Q与抗体的FC部分结合,就有两种相关的丝氨酸蛋白酶,称为C1R和C1s,变为活性并引发涉及其他补体蛋白的蛋白水溶性级联。经典途径是适应性免疫应答的体液臂的主要效应机制之一。先天免疫系统可溶性蛋白质称为五星素,也可以结合C1Q并引发经典途径。
另一种途径
稍后发现但是在典型的途径上被发现,当称为C3的补体蛋白直接识别出某些微生物表面结构,例如细菌LPS时,触发。C3还在溶液中以低水平体组成型活化并与细胞表面结合,但随后被哺乳动物细胞上存在的调节分子抑制。因为微生物缺乏这些调节蛋白,所以可以在微生物表面上扩增自发活化。因此,该途径可以基于调节蛋白的存在或不存在来区分正常的自我微生物。
章节途径
它由称为甘露糖结合凝集素(MBL)的血浆蛋白质触发,其识别在微生物糖蛋白和糖脂上的末端甘露糖残基,类似于前面所述的吞噬细胞膜上的甘露糖受体。MBL是Collectin家族(稍后讨论)的成员,其具有类似于补体系统的C1Q组件的六偏见结构。在MBL后结合微生物后,两个称为MASP1(甘露糖相关的丝氨酸蛋白酶1或甘油结合凝集素相关的丝氨酸)和MASP2的酶,其具有与C1R和C1S相似的功能,与MBL缔合,并引发与该MBL相同的下游蛋白水解步骤。古典途径。
补体激活的中心事件是补体蛋白C3的蛋白水解产生生物活性产物,随后C3的产物C3b与微生物细胞表面或与抗原结合的抗体共价结合。
补体激活取决于两种蛋白水解复合物的产生:C3转化酶,它将C3分解成两个蛋白水解片段C3a和C3b;和C5转换酶,将C5切入C5a和C5b。
启动途径有几件常见的事情。它们被触发
- 将它们的一个组分的结合到激活物中。
- 酶的级联激活
- 产生生物效应。
每种启动途径由不同类型的活化剂触发,通常是通过各个启动途径的组分“识别”的电荷图案的细胞,微生物或分子聚集体触发。
每个补体途径在起始步骤中都有独特的蛋白质,但在中间步骤中共享相同或相关的蛋白质,在最后步骤中使用相同的组分,最终达到相同的活性。补体激活代表了不同途径、控制过程以及其他蛋白质系统和细胞在局部环境中的动态相互作用。
补体激活促进了吞噬作用,因为C3b与微生物共价连接,而吞噬细胞(中性粒细胞和巨噬细胞)表达C3b的受体。C3(和其他补体蛋白)蛋白水解产生的肽刺激炎症。C5转化酶在上一代C3b之后组装,并且这种转化酶既有助于炎症(通过生成C5a片段),也有助于微生物靶点膜上孔隙的形成。补体激活的途径不同于C3b的产生方式,但在C5裂解后遵循一个共同的反应序列。


我可以在我的电子邮件ID上获取这些注释吗?