目录
什么是木质素?
- 木质素是一组复杂的芳族聚合物,由4-羟基苯基丙二醇的氧化组合产生。
- 木质素是一种酚醛聚合物,其是无定形的,不规则的三维和高分支。
- 木质素的生物合成方法是单体的自由基偶联反应形成交联酚聚合物。
- 木质素是木质纤维素生物质的重要组成部分,约占总重量的15-30%。
- 它是最丰富的芳族生物聚合物,由地球上约30%的有机碳组成。
- 化学物质如羟基肉桂醇(或单木质素醇),针叶树醇和sinapyl醇,通常有少量P.-Coumaryl酒精,被认为是木质素的主要建筑块。
- 然而,化学成分可能因物种而异。
- 名称木质素距第一次用于导出木质素和松柏醇单位之间的关系的拉丁字“利格纳姆”导出。
- 木质素是一个重要组成部分植物细胞壁在它提供结构支持的情况下,有助于水和营养物质的运输,并保护化学和生物攻击。
- 植物的多糖组分是高度疏水的,这允许通过像木质素这样的细胞壁组分运输水。
- 它有许多应用,包括能量生产,芳香化合物的生产,以及工业上重要的化合物的生产。
木质素的结构
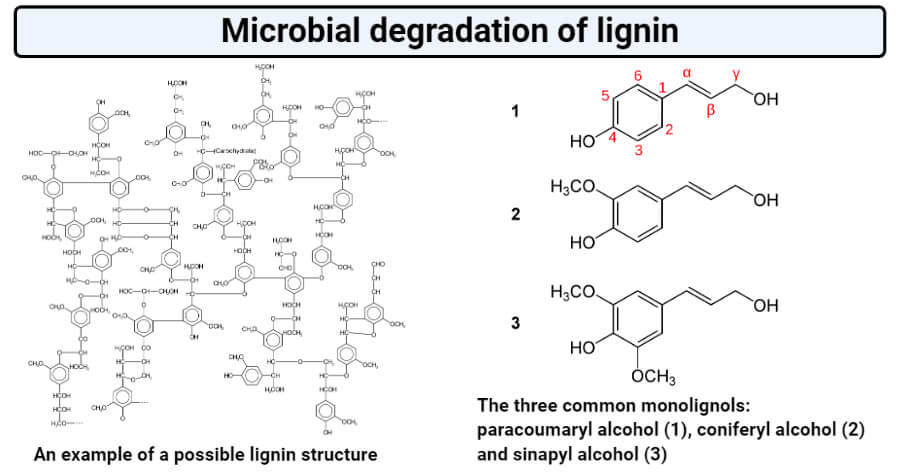
图:木质素的结构。图片来源:卡罗尔Głąb和yikrazuul.。
- 木质素由苯基丙烷单元通过烷基-烷基、烷基-芳基和芳基-芳基的化学键连接而成。
- 在自然界中木质素合成的前体包括对香豆素醇、针叶树醇和sinapyl醇。
- 不同的植物物种可能含有不同比例的前体,因为软木中的木质素主要由G-Unit组成,而在硬木和草本植物中分别由G-S单元和G-S-H单位组成。
- 天然木质素不是单体的简单连接,但它由不规则的偶联或添加前体形成。
- 不同组织或不同植物物种中木质素含量可能存在显着差异。
- 植物生长、营养、气候和光照等生态因子也影响木质素的化学结构。
- 木质素的化学结构是天然高分子领域中最具挑战性的问题之一。
- 木质素分子及其降解产物具有许多不对称中心,但不具有旋光性,因此它不是由单个键型连接构成的纤维素或蛋白质。
- 许多碳 - 碳键可能的结构单元之间存在的,和木质素的分子结构不能由一般的分解方法来确定。
- 因此,木质素是一类复杂的聚合物的分子结构,其不能通过结构式描述,并且木质素的性质仅基于元素,官能团及其在每个单元中的组合的基础上定义。
- 天然木质素由三种重要的元素组成:碳,氢和氧,其中碳含量远高于均质碳水化合物。
- 此外,木质素重要的结构特征包括官能团,包括醇羟基、羰基、羧基、酚羟基、甲氧基和磺酸。
- 木质素是受苯丙烷单元连接以形成经由各种化学键的三维结构木质素大分子。
- 苯丙烷单元间键的性质和相对比例是决定木质素化学结构的主要因素。
涉及木质素降解的微生物
- 木质素的生物降解是生物碳和氧循环中最重要的步骤之一。
- 多由植物生物合成木质素的矿化并返回到大气中CO2,但木质素分解的微生物学还不是很清楚。
- 目前已知的能降解木质素的微生物包括各种各样的真菌和细菌。
- 此外,含有蓝藻和放线菌等微生物也是为了降解木质素的微生物;然而,降解水平随微生物而变化。
- 木质纤维素废物的降解和转化归因于本地微生物的代谢。
- 不同的微生物种群在不同的阶段占主导地位,在有机物的降解过程中起着不同的作用。
1.Lignin-degrading细菌
- 木材的细菌降解通常缓慢发生,以及具有高水分含量的木材表面。
- 由于缺乏渗透能力,细菌通常与真菌同时侵入木细胞。
- 木质素降解酶的产生已被观察到结核分枝杆菌,M. vium,假单胞菌植物,P.铜绿假单胞菌,P. Putida,Bordetella Pertussis,Xanthomonas Campestris,大肠杆菌,Cahercacterus rodobacter capsulatus,yersinia pestis,夏季植物和嗜aeolicus。
- 细菌喜欢Paenibacillus.那Aneurinibacillus aneurinilyticus,芽孢杆菌sp。被发现降低硫酸盐木质素。
- 瘤胃细菌一样琥珀酸纤维杆菌,白色瘤胃球菌,flaavefaciens.是植物纤维细胞壁的主要降解,对木质素降解和生物产物形成的细菌具有新的作用。
2.木质素降解的放线菌
- 传统上,有人建议放线菌在木质纤维素沉积中发挥作用,但是用于这种击穿的规模和方法的细节较少。
- 链霉菌其他放线菌已被鉴定为木质素降解物种,可以从多种来源中分离出来,包括各种土壤、高温环境和白蚁内脏。
- 在五种不同的物种中观察到木质素降解的酶链霉菌;Streptomyces抗生素,S.Griseus,S. Coelicolor,S. cyaneus,和S. Lavendulae.。
- 过氧化物酶和多酚氧化酶的活性也观察到在嗜热链霉菌分离株和嗜苯胺链霉菌。
3.Lignin-degrading真菌
- 在不同的木材腐烂真菌中,只有白色腐烂有可能完全降解所有三个主要部件。
- 这些真菌主要属于ascometes,氘核菌或底霉素组。
- 白腐菌的典型例子有Ganoderma applanatum.和Heterobasidion annosum优先除去木质素而不纤维素的大量损失和引起白色口袋或腐烂的白色斑驳类型。
- 其他像子囊菌类茄丝核菌、斑点曲霉、鹅足孢、粗链孢、小麦禾麦酵母和trichoderma.reesei还描述了产生漆酶和其他木质纤维素酶。
- 在三个主要生态群中发现了木质素降解的重叠习惯,作为木材腐烂,菌根形成和凋落物分解真菌。
- 木腐烂真菌如亚hy族sp。(Nematolomasp),侧耳属sp。, 和蜜环菌还能够与木屑接触的土壤殖民化并导致木质素降解。
- Litter-decomposing真菌(如Stropharia rugosoannulata)能够在稻草上生长,这些稻草通常只能受到木材腐烂的真菌的青睐。
- Agaricus Bisporus.也是一种凋落物降解的真菌,其分泌漆酶和锰过氧化物酶,其分解木质素和纤维素的能力使其能够用作典型的白腐真菌。
参与木质素降解的酶
- 木质素不含水解键,这意味着酶必须具有氧化性质才能降解木质素。
- 木质素是一种立体不规则的化合物,这表明与其他天然聚合物相比,酶以一种更非特异性的方式攻击底物。
- 主要地,三种不同的酶参与木质素降解;锰过氧化物酶(MnP),木质素过氧化物酶(LIP),酶和漆酶。然而,许多其他酶参与木质素分解。
1.木质素氧化酵素(唇)
- 木质素过氧化物酶是一种含血红素的胞外过氧化物酶,依赖于H2O.2并降解各种木质素相关化合物。
- 这些酶具有异常高的氧化还原电位和较低的最适pH,通常对底物没有特异性。
- 木质素过氧化物酶是众所周知的两者的aphyllophoralic和agaricalic真菌所述木质素系统的一部分。
- 这些过氧化物优选氧化甲氧基化的芳香环没有游离的酚基团。
- 甲氧基苯并苯并和苄醇是木质素过氧化物酶最简单的芳族底物。
- 木质素过氧化物酶在木质素分解中的作用可能是锰过氧化物酶释放的木质素片段的进一步转化。
- 以商业化用于矿化以煅烧各种甲醛芳族化合物,如三环和四环多芳芳烃,聚氯氯联烯基和天然染料。
2.锰氧化物酶(MnP)
- 锰过氧化物酶是一种含细胞外血红素过氧化物酶,要求MN2+作为其还原性降低性质的底物。
- 锰过氧化物是由大多数木腐烂的真菌和许多凋落物分解真菌产生的最常见的木质素降解过氧化物酶之一。
- 在结构上,这些酶是糖基化蛋白质,具有铁原原卟啉IX(血红素)假体。
- 这种酶氧化锰2+对锰3+,这反过来将酚醛结构氧化给苯氧基自由基。m3+形成的是高度反应和络合物与螯合有机酸如草酸或苹果酸。
- 由于MnP-Mn络合物的氧化还原电位低于木质素过氧化物酶,故对酚类底物的氧化效果较好。
- 形成的苯氧基自由基可能进一步反应,导致了CO的最终释放2。
- 形成随后裂解Cα-Cα或引起解聚,以较小的中间体包括醌和羟基奎宁烷基 - 苯基键的苯氧自由基。
3.漆酶
- 漆酶是一组木质素降解酶,由n-糖基化的胞外蓝色氧化酶和活性位点上分布于不同结合位点的四个铜原子组成。
- 漆酶催化几种芳族氢供体的氧化,随后将氧还原到水。
- 此外,漆酶不仅氧化酚醛和甲氧基苯酚,还氧化它们并脱羧并攻击它们的甲氧基侧链或基团。
- 几种真菌漆酶已被认为在氧化还原介质存在的情况下氧化化合物,如1-(3,4-二甲氧基苯基)-2-(2-甲氧基苯基)丙醇-1,3-二醇(I)和酚木质素模型化合物,如酚红。
- 漆酶已被报道氧化许多顽固性物质,如氯酚多环芳烃(PAHs),木质素相关结构和有机磷化合物。
影响木质素退化的因素
木质素分解的方法可以通过许多类似的因素的影响;
1.水分含量
- 木质素的降解在源完全饱和且有游离水存在时发生得最快。
- 增加水的量,直到曝气受到损害对降解过程的影响不大。
2.增加了氮
- 木质素降解酶的生长和生物合成需要特定浓度的氮。
- 观察到,随着氮浓度的增加,木质素劣化的速率增加,但仅在一定程度上增加。
- 此外,添加非常高浓度的氮气倾向于对整个碳水化合物降解的碎屑作用以及木质素降解。
3.添加葡萄糖
- 木质素降解的过程随着葡萄糖的添加而减慢,因为葡萄糖等容易获得的能源导致木质素消耗降低。
- 当省略所有可用的能源,在富木质素化合物增加微生物的作用。
4.曝气
- 随着环境中氧含量的增加,木质素和碳水化合物代谢的速率增加。
- 这是由于涉及木质素劣化的大多数微生物是有氧微生物,其在高氧气气氛中茁壮成长。
- 此外,在CO作用下,木质素也能有效降解2浓度为30%的氧2浓度为10%。
- 然而,一个纯O2如果存在像葡萄糖或纤维素这样的其他形式的能量,则气氛可能是有毒的,因为它抑制木质素降解。
木质素降解的过程(简单步骤)
木质素分解的整个过程可以在两个简单的步骤进行说明;
1.解聚作用
- 木质素劣化的第一步是芳基和芳基化合物如β-芳基醚的解聚。
- 这一步骤是非特异性步骤,由不同的细菌和真菌酶在细胞外发生。
- 木质素的解聚是由β-O-4醚键裂解引起的,β-O-4醚键占木质素总键的50%或更多。
- 该步骤降低了木质素聚合物的长度,以获得二聚体或低聚单元,然后可以进一步降解到较小的分子中。
- 在微生物中解聚是通过在许多微生物如过氧化物酶和氧化酶苯酚发现不同木质素降解酶催化。
- 这些酶随机攻击木质素,然后将酚基转化为自由基,这些自由基导致木质素解聚。
2.溶解和矿化
- 解聚后形成的小分子木质素现在被不同的微生物所吸收,这些微生物通过各种体内酶催化一系列的转化。
- 大部分木质素分子之间的联系有其特定的代谢途径切割这些特定的联系。
- 矿化和低聚物和单体的溶解导致CO的形成2和其他可以被生物利用的必需分子。
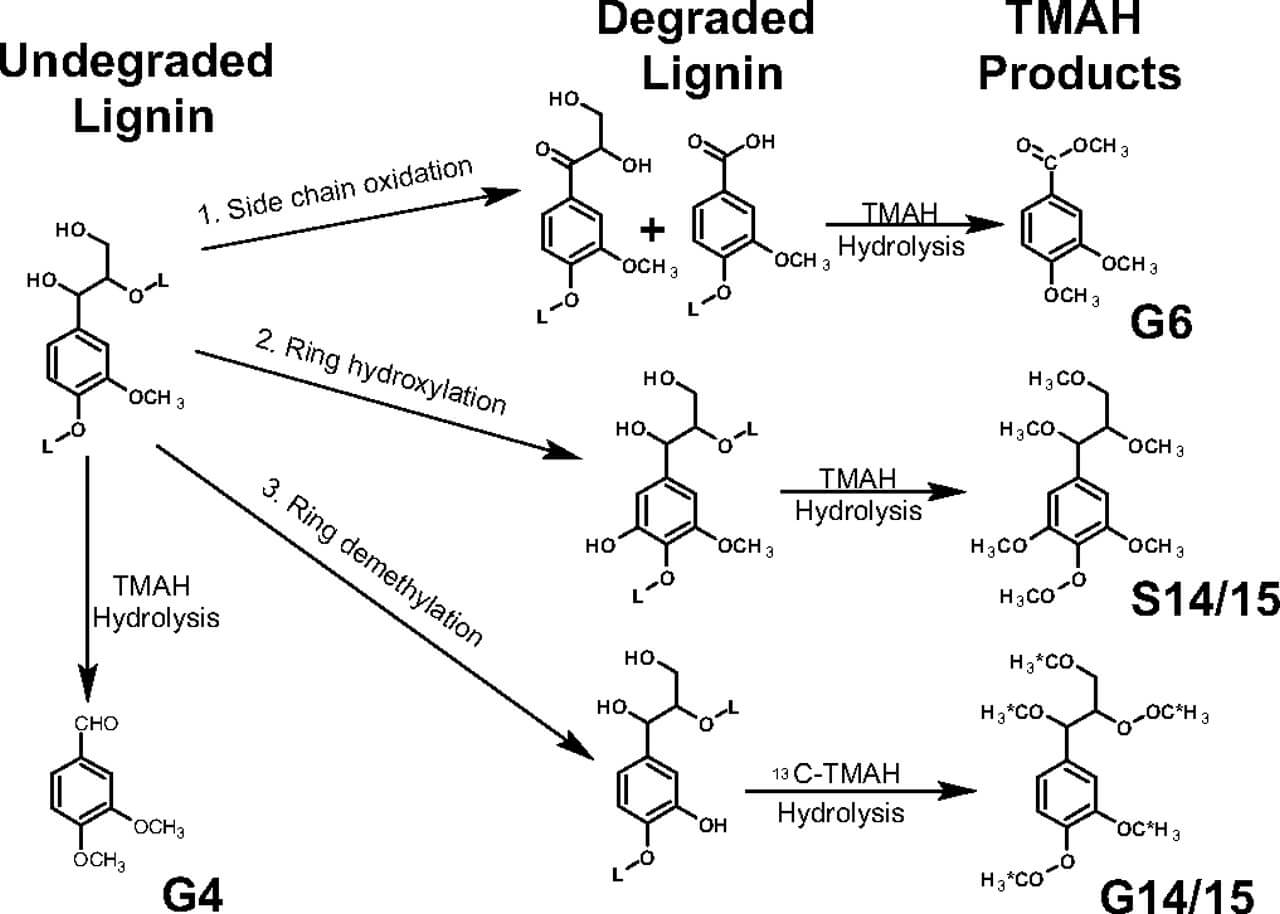
图:木质素生物降解反应。反应包括丙基侧链氧化/裂解(反应1)、环羟基化(反应2)和去甲基化(反应3)。反应1是白腐菌的特征,而反应2和反应3是褐腐菌的特征。每一个反应之后都有TMAH热化学分解的应用,显示了化合物G4, G6, G14/15和S14/15的化学结构,从这个分析结果。星号代表13由13C-TMAH分析。图片来源:https://doi.org/10.1073/pnas.0805257105。
木质素的微生物降解机制
- 木质素微生物降解的机制可能与涉及不同类型的酶不同。
- 三个特别重要的酶;漆酶和木质素过氧化物酶参与的木质素分子大的体外解聚。
- 其它机制参与木质素的溶解到微生物内甚至更小的可用的分子。
- 木质素降解的整个过程可以分为体外降解和体内降解。
A.体外降解
1.与漆酶的木质素生物降解
- Ligsin对碱素酶系统的生物降解是由酶催化和介质促进的自由基反应组成的氧化过程。
- 这一过程降解木质素中的酚类和非酚类芳香结构。然而,首先攻击的是酚基团,然后降解非酚基结构。
- 由于初始攻击,酚残基被氧化侧链释放。这使得酶能够穿透散装木质素聚合物,并充当天然介质以氧化非酚类区域。
- 通过非酚位点的Cα-Cβ裂解木质素分解所得的木质素与由亲水性木质素的介体复合物的形成木质素片段的增溶的机制。
- 这通过三个氧化机制之一;电子转移,自由基氢原子转移,和离子机制。
2.木质素过氧化物酶生物降解
- 木质素过氧化物酶样锰过氧化物酶的催化循环由H的结合引发2O.2或有机过氧化物转化为天然铁酶,形成过氧化物铁复合物。
- 这样形成的配合物被裂解,导致锰的氧化2+进入Mn.3+。
- 螯合物的锰3+与羧酸(如草酸、丙二酸、苹果酸)引起各种底物的单电子氧化。
- 通过除去氢化氢以形成苯氧基和氨基的酚类和氨基 - 芳族化合物。
- 这些基团是通过自催化反应产生的过氧化物来源,并且可以在没有外部H的情况下使用MNP2O.2。
- 木质素分解的潜在机制基于酶产生的Mn基于底物的初始单电子氧化3+,产生苯氧基自由基中间体。
- 这个自由基被Mn进一步氧化3+以形成一个碳中心阳离子。质子的后续损耗产生的酮二聚体。
- 水对阳离子的攻击,接着是芳基甘油-芳基结构的裂解,产生其他所描述的产物。
B.在体内降解
1.β-O-4醚降解
- β-O-4醚键的切割被认为是木质素脱聚的重要步骤,因为它占所有联动SIN木质素的约50%。
- 通路和β-O-4降解开始与LigD,一个Cα脱氢酶的机制。
- LIGD在Cα位置氧化羟基,然后将β-醚酶,LiGe或LigF氧化,切割β-O-4醚键并产生Vanillin和αGlutathional-β-羟基丙酮(GS-HPV)作为中间体。
- 最后,GS-HPV通过Ligg,谷胱甘肽-S-转移酶氧化。
- 谷胱甘肽被切割,其余β-hydroxypropiovanillone可进一步氧化到香草醛。
2.Bi-phenyl降解途径
- 联苯连接占软木木质素总连接的10%。
- 当5,5'-脱氢嘧啶(DDVA)进入生物,LIGX,DDVA O-脱甲基酶,将其移去甲氧基之一并将其转化为羟基。
- LigX的产物是LigZ, OH-DDVA双加氧酶的氧化间位裂解底物。
- 通过Ligz的产物通过Ligy水解,用于OH-DDVA的Meta-Cleavage化合物的水解酶。
- LigY裂解的最终产物为4-羧基-2-羟基戊二烯酸和5-羧基香草酸(5CVA),而5CVA进一步代谢为中心产物之一香草酸。
木质素降解的例子
木质素退化假单胞菌
- 假单胞菌在木质纤维素生物质中弥合各种低分子量脂质。
- 它产生苯甲醛裂解酶,其粘合1,2-二芳基乙烯化合物和苯并素的酰蛋白联系。
- 酶是高度特异性的,切割只anison(4,4'-二甲氧基安息香)和苯偶姻。
- 一些物种假单胞菌甚至可能产生原儿茶酸-4,5-双加氧酶催化的,其原儿茶酸和3-甲基 - 没食子酸的环裂变。
参考
- Kuhad R.C.,Kuhar S.,Sharma K.K.,Shrivastava B.(2013)涉及木质素降解的微生物和酶,营养富含动物饲料的生产:概述。在:Kuhad R.,Singh A.(EDS)环境管理和资源恢复的生物技术。印度兴趣者。https://doi.org/10.1007/978-81-322-0876-1_1
- 《木质素的生物合成与结构》。植物生理学153年,3(2010):895 - 905。doi: 10.1104 / pp.110.155119
- 安农齐亚塔,玛丽亚·格拉齐亚。“什么是木质素做的?新组件发现!”植物生理学180,3(2019):1255. DOI:10.1104 / PP.19.00561
- Vinardell,Maria Pilar和Montserrat Mitjans。“木质素及其对人体健康影响的衍生物。”国际分子科学杂志18日,6 1219。2017年6月7日,doi:10.3390/ijms18061219
- 王志强,王志强,王志强,等。木质素在纤维素中降解的影响因素Phanerochaete chrysosporium。拱门微生物137,171 - 175(1984)。https://doi.org/10.1007/BF00414462
- 杨H.H.,Effland,兆焦耳和柯克,T.K.(1980),在有代表性的木质纤维,热磨机械浆影响木质素的降解真菌因素。Biotechnol。生物工程,22:65-77。https://doi.org/10.1002/bit.260220106
- 齐默尔曼,沃尔夫冈。(1990)。木质素的细菌降解。生物技术杂志。119 - 130。10.1016 / 0168 - 1656 (90) 90098 - v。
- Hofrichter,Martin。(2002)。回顾:锰过氧化物酶(MNP)的木质素转化。酶和微生物技术。30. 454-466。10.1016 / s0141-0229(01)00528-2。
- 金,L.,尼古拉斯,D.D。与柯克,T.K。由固体基质条件下褐腐真菌中分离木质素的甲氧基碳的矿化。木头Sci.Technol。24,263-276(1990)。https://doi.org/10.1007/BF01153559
- Grzegorz Janusz,Anna Pawlik,Justyna Sulej,Urszulaświderska-Burek,Anna Jarosz-Wilkołazka,andrzejPaszczyński,木质素降解:微生物,涉及的酶,基因组分析和进化,有限元微生物学评价,第41卷,第6期,2017年11月,页941-962,https://doi.org/10.1093/femsre/fux049
- Chonlong基奥,莫伊妮塞恩,闻声秦。木质素利用率:从各种aspects.Renewable和可持续能源点评木质素解聚的审查。卷107页2019。232-249。https://doi.org/10.1016/j.rser.2019.03.008。
- Christopher Lew Paul,Yao Bin,Ji Yun。用漆晶晶介质系统生物降解。能源研究中的边疆。DOI = 10.3389 / FENRG.2014.00012
- 第二章木质素的结构与特性。木质素化学与应用。爱思唯尔》2019。25 - 50页。https://doi.org/10.1016/B978-0-12-813941-7.00002-3。
- Don L. Crawford,Ronald L. Crawford。木质素的微生物降解。酶和微生物技术。第2卷,问题1. 1980.第11-22页。https://doi.org/10.1016/0141-0229(80)90003-4。
来源
- 4%——https://www.sciencedirect.com/science/article/pii/B9780128139417000023
- 2% - https://www.sciencearirect.com/science/article/pii/s136403211930142x
- 2% - https://www.sciencearirect.com/science/article/pii/0141022980900034
- 2% - https://www.researchgate.net/publication/223374143_large_scale_production_of_manganese-peroxidase_using_agaric_white-rot_fungi
- 2%——https://www.researchgate.net/publication/222915661_Review_Lignin_conversion_by_manganese_peroxidase_MnP
- 1%——https://www.sciencedirect.com/science/article/pii/S0734975003001344
- 1% - https://www.sciencedirect.com/science/article/pii/s0141022901005282
- 1%——https://www.sciencedirect.com/science/article/pii/S0065216405580043
- 1% - https://www.ncbi.nlm.nih.gov/pmc/articles/pmc3825317/
- 1% - http://www.plantphysiol.org/content/153/3/895
- <1% - https://www.sciencearirect.com/science/article/pii/s0960852413005865
- < 1%, https://www.sciencedirect.com/science/article/pii/S0038071712002829
- < 1%, https://www.sciencedirect.com/science/article/abs/pii/S0958166909001268
- <1% - https://www.researchgate.net/publication/49647829_oxidation_of_polyclic_aromatic_hydrocarbons_by_the_bacterial_laccase_cueo_from_e_coli
- <1% - https://www.researchgate.net/publamication/35947053_degradation_of_recalcitrant_biopolymers_and_polyclic_aromatic_hydrocarbons_by_litter-decomposing_basidiomycetous_fungi
- <1% - https://www.researchgate.net/publication/329625877_advances_in_microbial_lignin_degradation_and_its_applications
- < 1%, https://www.researchgate.net/publication/251232174_Wood_Decaying_Fungi
- < 1%, https://www.researchgate.net/publication/223053539_Degradation_of_lignin_by_bacteria
- <1% - https://www.researchgate.net/publication/11833869_Fungal_Laccase_Properties_and_Activity_on_Lignin
- <1% - https://www.pnas.org/content/105/35/12932
- < 1%, https://www.jstage.jst.go.jp/article/pjab/80/5/80_5_204/_pdf/-char/en
- <1% - https://www.irjet.net/rachives/v7/i10/irjet-v7i10332.pdf
- <1% - https://www.chemguide.co.uk/mechanisms/freerad/allenehbr.html
- <1% - https://royalsocietypublishing.org/doi/10.1098/rsos.191202
- <1% - https://pubs.acs.org/doi/10.1021/bi047318e
- < 1%, https://onlinelibrary.wiley.com/doi/full/10.1111/j.1574-6968.2001.tb10911.x
- <1% - https://healthyeating.sfgate.com/three-elements-carbohydrate-including-sugar-8845.html
- <1% - https://gardenerdy.com/plant-growth-factors/
- < 1%, https://en.wikipedia.org/wiki/Lignin_biosynthesis
- < 1%, https://en.wikipedia.org/wiki/Lignin
- <1% - https://biotechnologyforbiofuels.biomedcentral.com/articles/10.1186/s13068-017-0735-Y
- <1% - https://aem.asm.org/content/68/3/1305
- <1% - http://web.nchu.edu.tw/pweb/users/taiwanfir/lesson/10476.pdf

