表的内容
Roantree等,介绍了一种分离β-溶血性链球菌的培养基。富含酵母核酸和麦芽糖的中富含菌落尺寸增加,增强了这些生物产生的溶血性和敏感区的清晰度。链球菌选择琼脂是推荐用于a组初步分离的选择培养基链球菌物种 (S. pyogenes)来自口服培养和呼吸样本。它设计用于抑制革兰氏阴性杆菌和葡萄球菌,从而允许分离,传代培养和鉴定病原链球菌,包括β-溶血性链球菌和S.肺炎。
作品
| 原料 | 克/ L. |
| 酪蛋白蛋白胨 | 15.0克 |
| 大豆饭的消化不良 | 5.0 G. |
| 氯化钠 | 5.0 G. |
| 核酸 | 3.0 G. |
| 麦芽糖 | 0.5克 |
| 新霉素 | 10.0毫克 |
| 多粘菌素B. | 10.0毫克 |
| 羊血 | 50.0毫升(5%) |
| 琼那 | 15.0克 |
最终pH 7.3 +/- 0.2,25ºC。
原则
有机氮的营养来源,特别是细菌生长所需的氨基酸和长链肽,由酪蛋白和大豆蛋白胨的组合提供。这种组合使得培养基营养丰富。氯化钠维持介质的渗透平衡。核糖核酸和麦芽糖促进溶血的产生。添加羊血(5%)可为挑剔的微生物提供额外的生长因子,并有助于确定溶血反应。选择性药物如新霉素和多粘菌素B被添加到抑制共生口腔菌群,包括大肠菌群、葡萄球菌、微球菌那嗜血杆疮,和奈瑟氏菌属物种。
的制备链球菌选择性agar.
- 将组件除外羊血液,麦芽糖溶液和抗生素添加到蒸馏水/去离子水中,并将体积带到930.0ml。
- 彻底混合。
- 轻轻地加热并带来沸腾。
- 在15psi压力- 121°C下高压釜15分钟。
- 冷却至45°-50°C。
- 无菌添加无菌羊血、无菌麦芽糖溶液、无菌抗生素抑制剂。
- 彻底混合。
- 倒入无菌培养皿或放入无菌试管中。
结果和解释
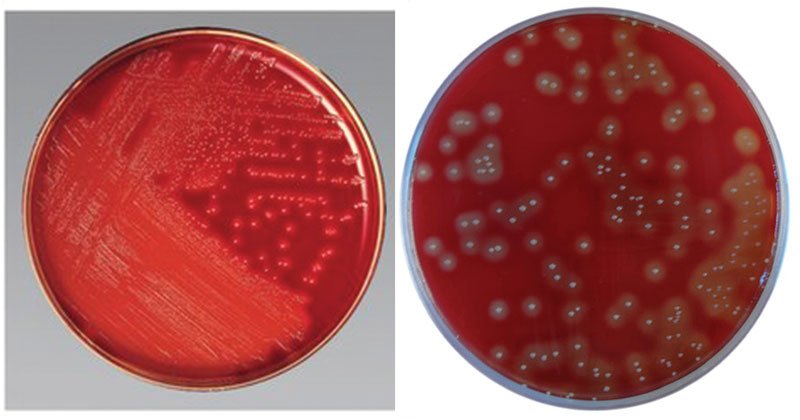
- 在富含二氧化碳的气氛中培养18-48小时后,平板显示条状区域的分离菌落和大量接种区域的融合生长。
- 组链球菌(S. pyogenes)将显示为半透明或不透明,白色到灰色,小(1至2毫米)菌落包围,被β溶血区域包围。
- 针对α,非溶解或其他β-溶血链球菌的定位或非常小的菌落可能以少量生长。
- 奈瑟氏菌属除A组和B组外,绿链球菌、葡萄球菌、革兰氏阴性杆菌和大多数乙型溶血性链球菌在培养基上受到抑制。
使用
- 链球菌设计了用于呼吸道A群链球菌初步分离的选择性琼脂。
- 它也可以在孤立的隔离中使用链球菌,包括甲组链球菌(S.pyogenes.)、B (美国agalactiae), C, D, F, G,和S.肺炎,特别是来自呼吸样本。
限制
- 一些群体的链球菌(S. pyogenes)可能会遇到在这种媒体上会变得不佳;标本的性质和生物体的生理状态可以影响所需物种的恢复,以及改变该培养基的抑制特征的影响。因此,非选择性控制的检查并将它们与选择性培养基进行比较以获得其他信息,并确保建议使用任何潜在病原体的最佳恢复。
- 建议进行额外的生化检查和血清学检查以作最后确认。
- 应该认识到,通常易于在选择性培养基中易于抗微生物剂的生物可以完全或仅部分地抑制因子浓度,微生物菌株的特征和接种物中的生物的数量。不应抑制通常耐抗微生物剂的生物。因此,在选择性培养基上生长的标本的培养物应与在非选择性培养基上培养的标本进行比较,以获得其他信息,并有助于确保潜在病原体的恢复。
- 已经显示出D组群组株菌株的溶血反应受动物血液差异的影响。这些菌株是在马,人和兔血糖和羊血琼脂上的β-溶血性β-溶血性。
- 已知孵育气氛影响溶血链球菌的溶血反应。为了获得最佳性能,在增加的CO2(5 - 10%)下按照建立的实验室程序培养血琼脂基础培养基。
参考文献
- Himedia
- 贝克顿,迪金森,还有他们的公司
- 哈代的诊断
- Thermofish.
- 新生公司
- Lowbury EJ,Kidson A,Lilly Ha(1964年)。一种新的选择性血液琼脂培养基酿脓链球菌和其他溶血链球菌。J Clin Pathol.。17(3):231-235。
- Bellon J,Weise B,Verschraegen G,De Meyere M.选择性链球菌琼脂与血液琼脂检测急性咽炎患者β-溶血链球菌的检测。J Clin Microbiol.。1991年; 29(9):2084-2085。

