目录
T细胞(T淋巴细胞)定义
胸腺来源的淋巴细胞或T细胞是免疫系统的细胞,是适应性免疫系统的重要组成部分。
- 这些是血细胞(白细胞),根据被激活的T细胞的类型,攻击入侵的病原体和宿主细胞。
- T细胞不同于其他淋巴细胞,因为T细胞表面有T细胞受体,而其他淋巴细胞没有。
- T细胞是适应性免疫应答中的关键因素之一,因为受体与MHC络合物相互作用暴露于抗原呈递细胞抗原.能激活T细胞反应的抗原范围在不同的生物体中是不同的。
- T细胞可以与其他淋巴细胞区分开B细胞随着T细胞的成熟和分化发生在胸腺中。
- 存在不同的T细胞子集,其涉及细胞的不同功能。这些细胞是免疫介导的细胞死亡的主要原因。
- T细胞在生产中产生骨髓这一过程是由一组被称为调节性T细胞的T细胞控制的。
- T细胞是适应性免疫系统的一部分,有一组随机产生的膜受体来遇到抗原。
- T细胞也不同于B细胞,因为T细胞不能作为抗原提呈细胞,需要通过抗原提呈MHC分子.
- T细胞约占血液中淋巴细胞总数的60-70%,但与B细胞相比,很难分离和定义T细胞。
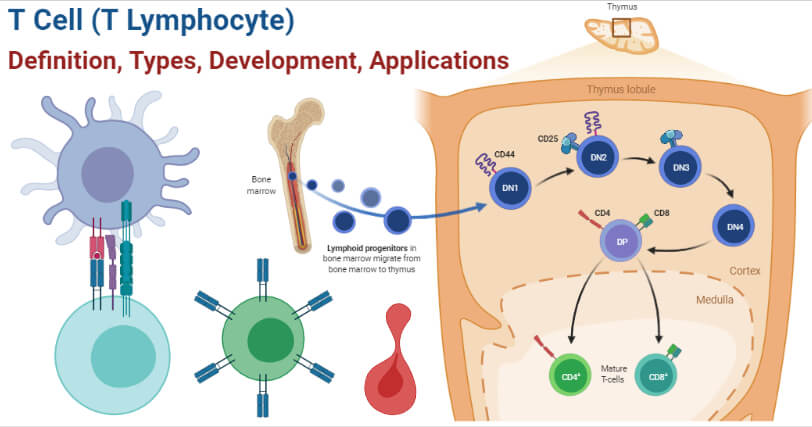
T细胞(T淋巴细胞)类型
T细胞主要根据它们的功能被分类。定义这些类别的其他因素是基因或蛋白质表达模式。以下是不同类型的T细胞;
辅助T细胞(CD4+T细胞)
- 辅助CD4+T细胞或辅助T细胞是帮助B细胞等其他淋巴细胞成熟并分化为浆细胞和记忆B细胞的淋巴细胞。
- CD4.+通过II类MHC分子激活T细胞,其在其膜上存在的CD4受体之后命名。
- 辅助T细胞约占T细胞总数的50-60%,然后进一步激活其他免疫细胞来保护身体免受外来颗粒的攻击。
- CD4的激活+T细胞导致细胞的分化和细胞因子的分泌以调节整体免疫应答。
- 这些细胞可以进一步分化为其他亚型,这取决于产生的细胞因子的类型。
- 辅助T细胞的两个亚群是Th1和Th2细胞,它们基于参与T细胞激活的toll样受体类型。
- Th1细胞通过增加细胞的吞噬活性参与对病原体的攻击巨噬细胞,而Th2细胞参与B细胞的激活。
- Th2细胞也参与其中调理素作用在那里,它们覆盖在病原体的表面以诱导吞噬作用.
2.细胞毒性T细胞(CD8+T细胞)
- 细胞毒性T细胞或CD8+T细胞是I类MHC分子在抗原呈递细胞上激活的T细胞。
- 它们被命名为CD8+T细胞,因为它们含有表面上的CD8受体。受体以总T细胞的约40%存在。
- CD8+T细胞被激活后,通过无性繁殖的过程分化为细胞毒或杀伤T细胞。
- 细胞毒性T细胞通常破坏病毒感染的细胞或肿瘤细胞以及参与移植物的细胞。
- 这些细胞通过与I类MHC分子一起出现的短肽结合来识别目标细胞。
- 细胞毒性T细胞还分泌IL-2和IFN-γ等细胞因子,调节其他免疫细胞的效应功能。
3.内存T细胞
- 由于MHC分子遇到完整的抗原,记忆T细胞是由幼稚T细胞分化的细胞。
- 内存T细胞是一类长寿命的T细胞,并且当重新暴露于首先激活它们的抗原时,可以快速扩展到大量的效应器T细胞中。
- 这些细胞可以表达任何一种CD4+和CD8+受体但更常见的是,这些表达CD45RO。
- 存储器T细胞可以进一步分为中央存储器T细胞,效应存储器T细胞,组织驻留存储器T细胞和虚拟存储器T细胞等亚型。
- 中央记忆T细胞通常表达CD44,可以在其中找到淋巴结和外围循环。
- 效应内存器T细胞表达CD45RO并保留在周围循环和组织中。这些细胞在特定抗原存在下终止于效应器T细胞。
- 虚拟记忆T细胞不同于其他记忆T细胞,它们不是克隆扩增的结果。这些细胞数量相对较少,大多留在外周循环中。
4.监管CD4.+T细胞
- 调节性T细胞是涉及维持免疫反应和耐受的T细胞。
- 这些细胞主要在免疫反应结束时关闭T细胞介导的免疫,同时也抑制在阴性选择过程中逃避激活的自体反应T细胞。
- 监管性T细胞是两个类CD4+调节性T细胞;FOXP3+ T细胞和FOXP3- T细胞。
- 该组调节性T细胞可以在胸腺中的T细胞发育的正常过程中形成或外围诱导。
- 在胸腺中形成的调节细胞称为胸腺Treg细胞,诱导细胞称为外周衍生Treg细胞。
- 这两类调节性T细胞都需要转录因子FOXP3的表达,FOXP3也被用于识别这些细胞。FOXP3基因的突变会影响调节性T细胞的发育,导致自身免疫疾病.
T细胞(T淋巴细胞)发育
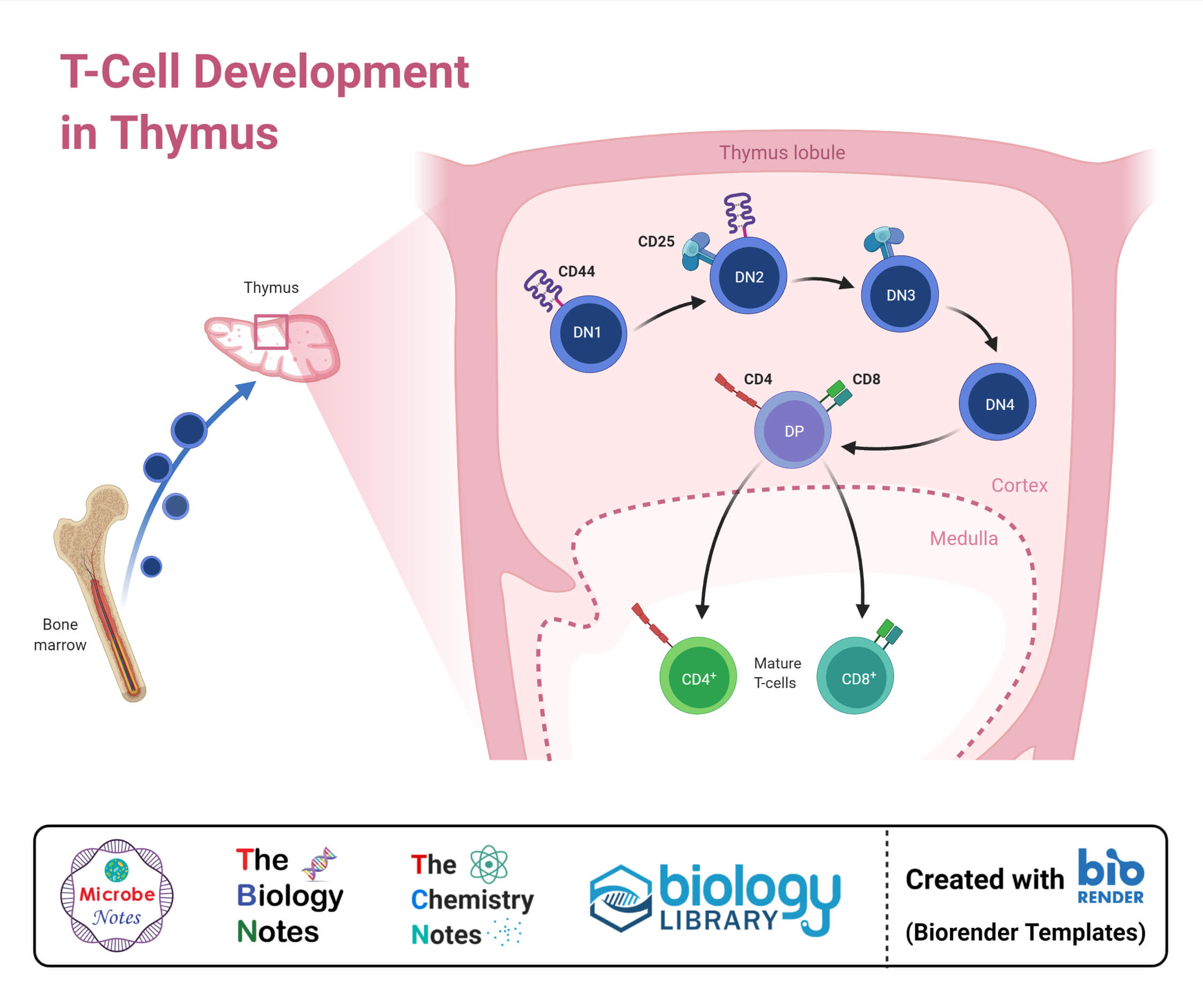
- 与所有其他血细胞一样,T细胞源自骨髓中存在的造血干细胞。在某些情况下,在胚胎发育期间,发展可能在胎儿肝脏中开始。
- 然后这些细胞发展成多能的祖细胞,保留了分化成髓细胞和淋巴细胞的能力。
- 进一步的分化导致形成可分化成T,B或NK细胞的常见淋巴祖细胞。
- 在T细胞的情况下,共同的淋巴祖细胞通过血液移动到胸腺,在那里它们被移植。
- 达到胸腺的细胞称为双阴性细胞,因为这些不表达任何CD4或CD8共受体。
- 胸腺中的细胞不能自我更新,胸腺生成(T细胞的形成)依赖于从骨髓中不断招募细胞。
1.成熟
- 进入胸腺的细胞在发展为早期胸腺祖细胞(ETP)之前遇到胸腺上皮。这一阶段的细胞为CD4-、CD8-、CD44+ CD25-和ckit+细胞。
- 胸腺中的微环境限制了这些细胞向髓细胞和直流电细胞转化的潜能。
- 胸腺由四个主要隔间组成,其中每个主要隔室具有不同的功能,并调节T细胞开发的不同阶段。
- 这些隔室是囊下带、皮质、髓质和皮质髓质交界处。
- 胸腺细胞的发育在胸腺的不同区域经历了不同的阶段,可以通过分子的细胞表面标记表达的改变来追踪。
- 双阴性(DN)细胞可进一步分为四个不同的阶段,并根据其缺乏受体而被识别。
- DN1细胞是表现出高CD117水平的ETPs,约占胸腺T细胞总数的0.01%。DN1细胞从皮质髓质连接处向深层皮质向囊下区移动。
- 在这里,细胞分化为DN2胸腺细胞,包括CD24+、CD25+、CD44+和CD117+细胞。然后DN2胸腺细胞经历基因重组和分泌细胞因子,如IL-7。
- 细胞进一步分化为DN3阶段,其中T细胞表达了称为Pre-Tα的不变α链。基因的排列与不变链一起产生信号以进行T细胞成熟的过程。
- 在DN3阶段,细胞成熟为DN4,并进一步上调为CD4和CD8细胞,在成熟过程中达到双重阳性状态。
- αβ T细胞受体的特异性和结合强度决定了细胞的存活和分化。
- 这个过程之后是两个不同的过程;积极选择和消极选择。
一个积极的选择。
- 阳性选择是双阳性T细胞(CD4)的运动过程+和CD8+)到皮质,在那里遇到自我抗原。
- 胸腺皮层上皮细胞在MHC分子上表达自身抗原,T细胞与MHC分子相互作用。与MHC细胞有高度亲和力的细胞存活下来,而与分子没有足够强相互作用的细胞存活下来。
- 在此过程中发生的大部分显影胸腺细胞,持续多天。
- 在阳性选择中,CD4+细胞与类MHC分子相互作用,而CD8+细胞与II类MHC分子相互作用良好。
湾否定选择
- 在阳性选择中存活下来的细胞进入髓质并进行阴性选择,这将消除对自身抗原具有高度亲和力的胸腺细胞。
- 与自我抗原相互作用的细胞接受凋亡信号导致细胞死亡。
- 然而,在同样的过程中,一些细胞被选择形成Treg细胞。成功完成选择过程的细胞以成熟的naïve T细胞的形式离开胸腺。
2.激活
- 成熟的naïve T细胞离开胸腺,进入血液,在那里循环,直到它们在抗原提呈细胞表面识别出自己的特定抗原。
- CD4的激活+细胞是T细胞受体和T细胞上的共刺激分子(CD28或ICOS)相互作用的结果。
- CD4的激活+细胞对于幼稚CD8T细胞和记忆T细胞的初始抗原活化是必不可少的。
- 初始信号通过T细胞受体与II类MHC上存在的同源肽的结合提供。在II类MHC上存在类似的肽,其激活CD8+细胞。
- 作为共刺激提供的第二信号,其中表面受体通过相对少量的刺激诱导,该刺激是病原体或细胞分解产物的产物。
- NaïveT细胞仅表达CD28作为共刺激受体,其与APC上存在的CD80和CD86蛋白质相互作用。
- 两步激活过程可防止对自我抗原的不当反应,因为自肽不提供合适的共刺激。
- 在这两种信号之后,T细胞也会受到细胞因子的刺激。细胞因子信号决定了T细胞的命运,尤其是辅助T细胞。
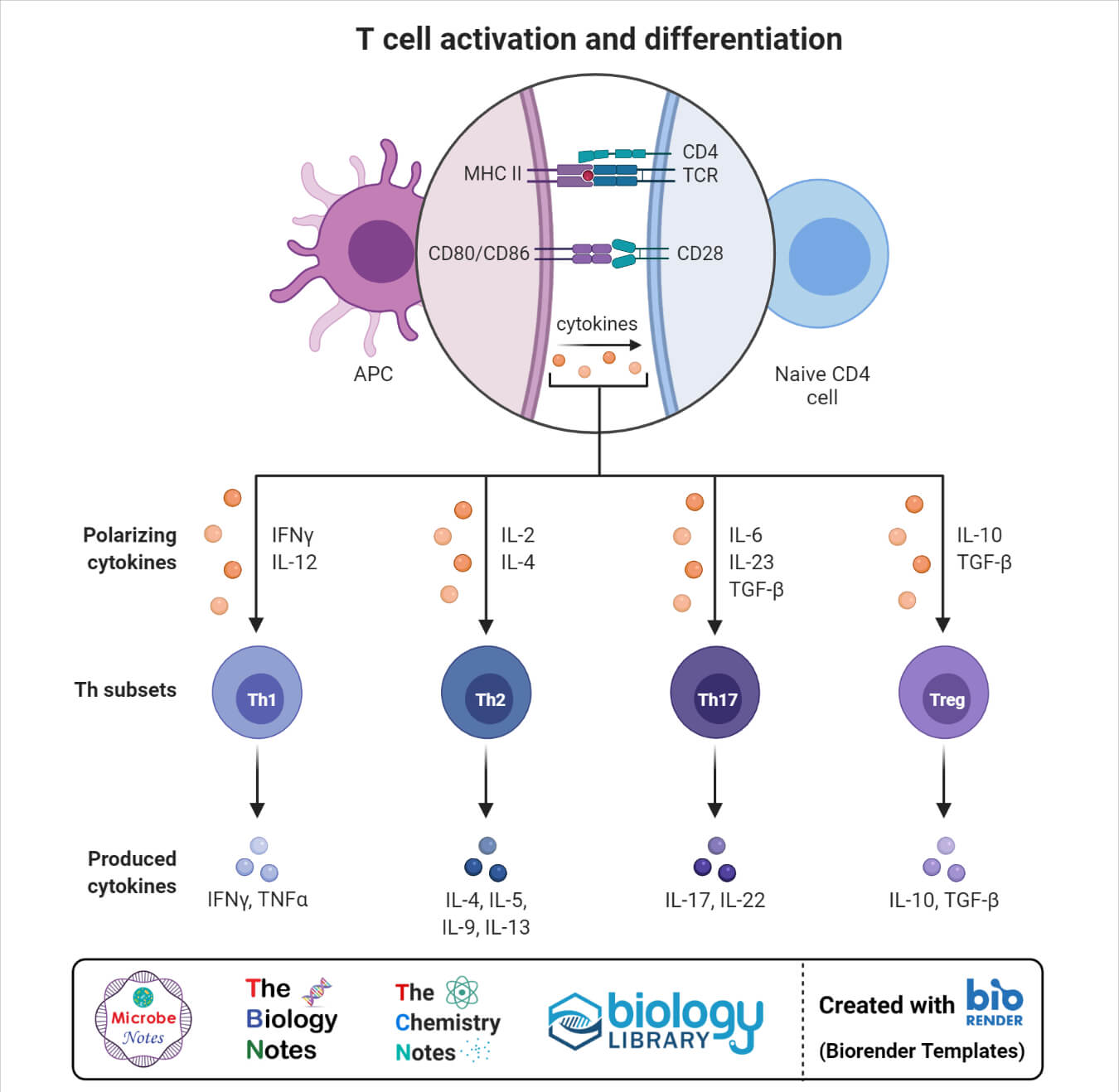
3.分化
- T细胞分化成不同类型的T细胞通常以谱系承诺的形式发生,所述谱系的形式是基于T细胞受体对自抗原的亲和力。
- 该决定是在双阳性胸腺细胞阶段进行,其中细胞确定是否加入CD8+细胞毒性T细胞或CD4+辅助T细胞。
- 这些谱系承诺需要改变基因组组织和基因表达,导致基因的沉默和与特定谱系功能相关的基因的表达。
- 确切的分化模式尚不清楚,但最新的解释这一谱系的模型表明,它是基于两个MHC类之一的亲缘关系。
T细胞(T淋巴细胞)应用
作为免疫系统的一部分,T细胞有不同的功能和用途,可以用来保护身体。以下是该等申请的一些用途;
嵌合抗原受体(CAR) T细胞治疗
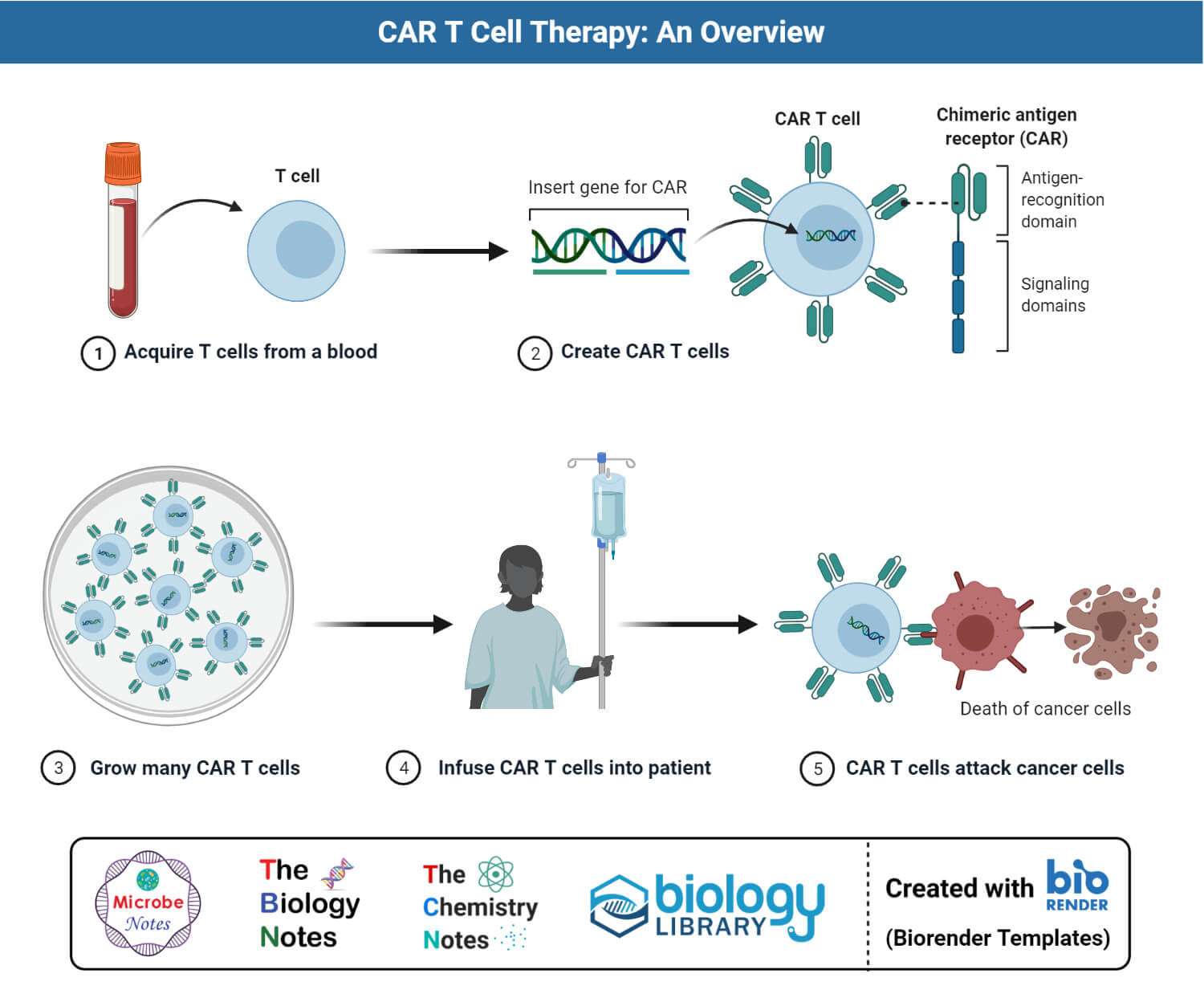
数字:嵌合抗原受体(CAR) T细胞生成和癌症治疗的逐步概述。
- 嵌合抗原受体(CAR) T细胞治疗是一种很有前途的免疫治疗方法癌症这涉及到使用工程嵌合抗原受体将T细胞定向到靶向的恶性细胞。
- CAR - T细胞疗法已经成功地用于治疗血液系统恶性肿瘤的临床试验。
- 用作靶的抗原是CD19,其通常在前体上表达,并且成熟的B细胞也可用于治疗B细胞恶性肿瘤。
- 该技术也可以用于实体肿瘤,但效率不如血癌治疗的情况下。
参考
- Peter J. Delves, Seamus J. Martin, Dennis R. Burton和Ivan M. Roitt(2017)。Roitt的基本免疫学,第十三版。约翰瓦里和儿子有限公司
- Judith A. Owen, Jenni Punt, Sharon A. Stranford(2013)。Kuby免疫学.第七版。w·h·弗里曼公司。
- T细胞发育和转化的机制。Cell Dev Biol. 2011;27:539-62。doi: 10.1146 / annurev - cellbio - 092910 - 154008。2011年7月5日。PMID: 21740230。
- Alberts B,Johnson A,Lewis J等人。细胞的分子生物学。第四版。纽约:花环科学;2002. T细胞和MHC蛋白。可从:https://www.ncbi.nlm.nih.gov/books/NBK26926
- Kumar, Brahma V等,《人类T细胞的发育、定位和整个生命中的功能》。免疫力卷。48,2(2018):202-213。DOI:10.1016 / J.IMMUNI.2018.01.007
- Zijun Zhao,Yu Chen,NgiamBudulu M. Francisco,袁清张,闵豪吴。Car-T细胞疗法在血液恶性肿瘤中的应用:优势与挑战。Acta Pharmaceutica Sinica B.第8卷,第4版2018.第539-551页。https://doi.org/10.1016/j.apsb.2018.03.001。

