CADD具有选择性高、效率高、疗效好、持续时间短、毒性低、与各种药代动力学参数拟合较好等特点,备受关注(Makrynitsa et al., 2018)药物化学与生物活性之间的平衡是有效药物设计的关键。随着对药物需求的不断增长,生物活性结构的选择越来越受到人们的关注。结构生物学的知识和计算机的力量已成为可能,利用计算方法来识别活性文库,以解决分子肥胖问题。
表的内容
什么是计算机辅助药物设计(CADD)?
CADD的主要目标是筛选、优化和评估化合物对目标的活性。它形成了学术和主要制药公司的多学科方法,以更好的疗效,没有/更少的副作用。CADD的进展是基于相似度、靶点识别、结构预测、结合位点/空腔、验证、了解蛋白质-配体相互作用以及筛选大量化合物,掌握基于生理条件的分子动力学模拟,计算ADMET性质,利用QSAR(定性结构基础评估关系)估计先导化合物的生物活性,以获得更好的疗效和选择性。
基于计算机辅助药物设计的药物清单
| 药物 | 疾病 | 目标 |
| 羟吗啡酮 | 阿片类镇痛药 | 情绪受体激动剂 |
| Saquinavir | 艾滋病 | 抑制HIV1和HIV 2的蛋白酶 |
| 卡托普利 | 高血压或高血压 | 抑制血管紧张素转化酶的转化 |
| 扎那米韦 | 影响甲型流感和乙型流感 | 抑制神经氨酸酶 |
| Dorzolamide | 青光眼和高眼压 | 抑制碳酸酐酶 |
类型的CADD
A.基于结构的药物设计(SBDD)
什么是基于结构的药物设计?
基于结构的药物设计(SBDD)是管理整个药物开发的最有效和最有力的过程。小分子靶点信息、基因及其序列信息、结合信息、细胞毒性、吸收、代谢、排泄(ADMET)数据等重要的生物学信息是加速药物发现过程的最有效来源。这已经成为一种很有前途的计算技术,被各种研发和制药公司使用。该管道将涉及结构预测、可视化、结合位点表征、分子对接和虚拟筛选、对接络合物结构的可视化及其稳定性分析、ADMET筛选和结合自由能- MM PBSA。
基于结构的CADD的步骤或过程
- 蛋白质结构的测定
- 比较建模
- 装订袋标识
- 得分函数
- 知识得分
- 部队得分函数
- Protein-ligand对接算法
- 虚拟筛选
- 蛋白质配体图的可视化。
基于结构的药物设计软件(SBDD)
SBDD方法中的工具和应用程序列表
| 阶段 | 工具使用 | 简要描述 | 链接 |
| 1.目标建模 | 瑞士模式 | 同源性建模 | 瑞士模式(expasy.org) |
| MODELER | 同源性建模 | 分析员(salilab.org) | |
| Phyre和Phyre2 | 模板检测对齐以及三维建模 | PHYRE2蛋白质折叠识别服务器(原英国) | |
| HHpred | 模板检测、对齐和3D建模 | 用于蛋白质同源性检测和结构预测的HHpred交互服务器| HSLS (pitt.edu) | |
| I-TASSER | 线程从头开始建模 | 蛋白质结构和功能预测I-TASSER服务器(zhanggroup.org) | |
| 2.结合位点 | CASTp | 结合位点预测 | CASTp 3.0:蛋白质表面形貌计算图谱(uic.edu) |
| 主动站点预测工具 | 活性位点预测 | ACTIVE SITE PREDICTION SERVER (scfbio- itit .res.in) | |
| 3.分子对接 | AutoDock维纳 | 分子对接和虚拟筛选 | AutoDock维纳(scripps.edu) |
| 薛定谔 | 大师 | 大师| Schrödinger (schrodinger.com) | |
| 4.ADMET预测 | admetSAR | ADMET预测 | ADMET计算工具(osdd.net) |
| QIKPROP | ADME分析 | QikProp | Schrödinger (schrodinger.com) | |
5.分子动力学模拟 |
琥珀色的 | 执行生物分子模拟程序 | www.gromacs.org |
| GROMACS | 通用分子动力学模拟程序 | https://www.gromacs.org | |
MM-PBSA |
g_mmpbsa |
该工具使用MM-PBSA方法计算结合能 | ambermd.org |
空腔结合部位及预测:
在蛋白质配体复合体的三维结构中,最可靠和准确的区域是对a区域的分析和预测蛋白质配体可以占据最佳位置。一些空腔预测工具,如Castro, Q-site Finder和COACH,可以提供蛋白质结合位点的可能位置。这些工具是基于进化的、基于能量的或基于几何的方法设计的。基于进化的方法获取所有相关蛋白质的信息,并显示几乎相同的结合位点。基于几何的方法是基于特征,如形状、疏水表面和带电表面残基,而基于能量的方法使用探针来识别蛋白质上的有利结合区域。
基于结构的药物设计实例(SBDD)
在SBDD中列出重要的数据库资源
| 数据库 | 描述 | 链接 |
| Chemspider | 配体结构 | ChemSpider |搜索和分享化学 |
| PubChem | 小分子和生物活性的数据库 | PubChem (nih.gov) |
| DrugBank | FDA批准了药物再利用 | 药物银行在线|药物和药物靶点信息数据库 |
| 锌 | 该数据库为虚拟筛选和分子对接提供了化合物 | 锌(docking.org) |
未来的角度
人工智能和机器学习与基于结构的技术的结合成为了一种新的工具,在发现治疗学方面具有巨大的潜力。也许,科学界必须克服与算法、评分函数和现有数据的可用性相关的可能性。这一基本平台的形成加速了临床试验,限制了有前途的候选药物的失败。随后,SBDD将成为一种新的、可靠的、高效的药物设计技术。
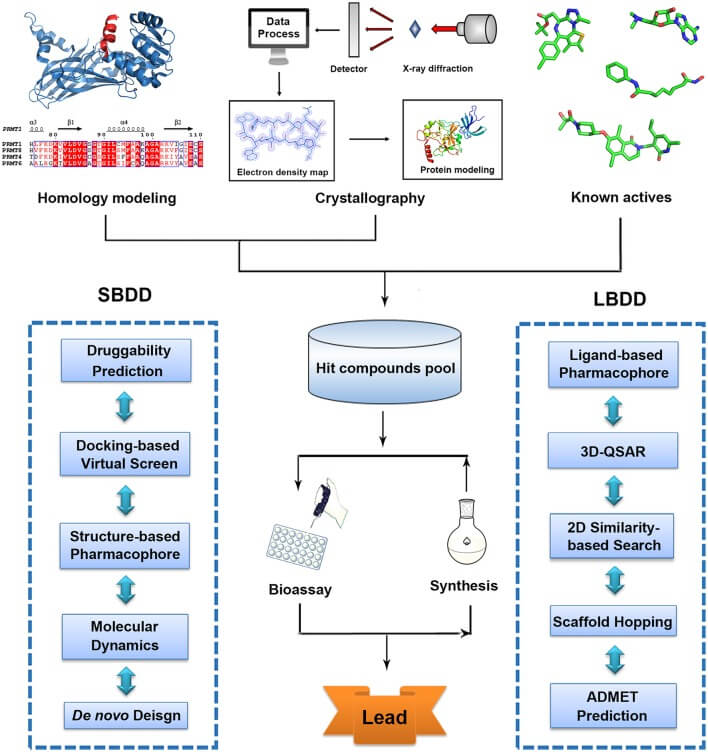
B.配体药物设计(LBDD)
什么是配体药物设计(LBDD)?
三维大分子结构的缺乏导致非常系统的目标识别使用先进的计算工具。目前,医药科研人员在这方面面临着更加严峻的形势和重大挑战。高通量筛选(HTS)的假设已经通过更好的新兴策略得到了加强。间接药物设计模式或配体药物设计广泛支持这一更艰巨的挑战。这可以通过三种不同的方式来实现,例如
- 机器学习方法
- 相似性搜索方法
- 药效团模型映射
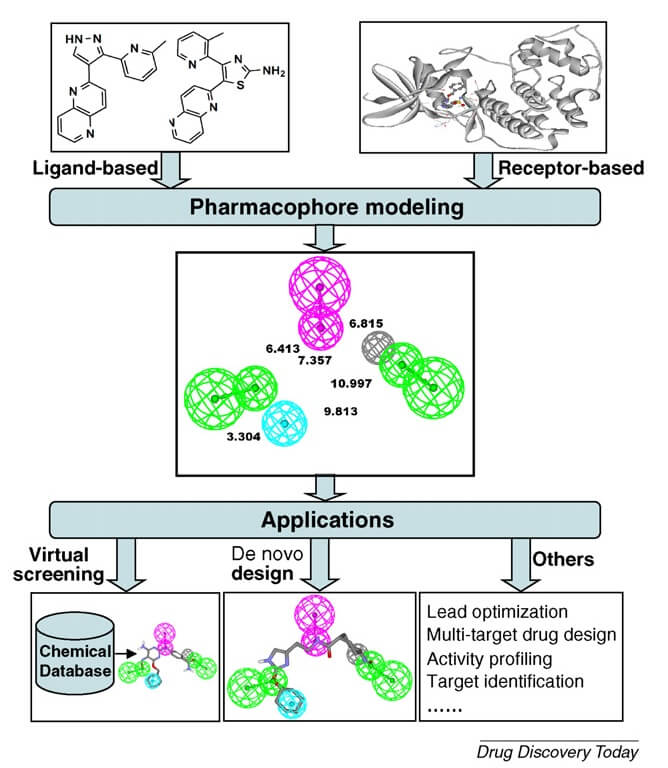
药效团模型映射
该方法被用于医学和计算化学领域的先导优化。它建立在使用结构对齐和预测活动和三维数据库搜索的基础上。用于发展分子结构及其对任何目标的活性的已知/未知数据集的数量。这可以在ADMET分析、副作用估计、脱靶预测等领域中体现出来。利用药效团的知识,通过虚拟筛选改进了模拟研究。
药效团建模的基本步骤
- 不同的结构和适当定义的实验活动
- 代的构象
- 采用三维药效团模型,分三个阶段建立化合物的训练集
- 构建期:药效团模型建立在常见活性分子上
- 减法阶段:不同于药效团模型的减法
- 优化阶段:通过优化模型生成假设
- 质量评价:药效团的选择以成本函数为基础
- 验证
- Fisher的随机化检验是对一组经过验证的化合物进行的
- 最后,对化合物的测试集进行映射。
用于药效团建模和应用的工具
S.No |
工具 |
描述 |
链接 |
1. |
制药 | 该工具使用化合物进行虚拟筛选 | 欢迎光临ZINCPharmer (pitt.edu) |
2. |
Pharmapper | 它意味着超过7000个基于靶标的药效团模型的知识,并提供了输入配体与药效团模型的最佳匹配。 | 欢迎来到我们的实验室。 |
3. |
药剂师 |
该工具在没有目标的情况下从一组配体中搜索 | BioInfo3D集团(tau.ac.il) |
4. |
Pharmit工具 |
这依赖于药物动力学的药物监测 |
Pharmit:化学空间的互动探索(pitt.edu) |
5. |
发现工作室 | 用于治疗和药物监测的工具 | 免费下载:BIOVIA Discovery Studio Visualizer -达索Systèmes (3ds.com) |
6. |
Ligandscout |
它从分子训练/测试集的结构数据中建立3D药效团模型 | Linux |
7. |
阶段 |
该工具考虑了配体和基于结构的药物设计 |
Schrödinger | Schrödinger是开发用于制药、生物技术和材料研究的最先进的化学模拟软件的科学领导者。(schrodinger.com) |
铅分子的发现
具有治疗特性的生物学或药理特性的化合物可称为先导分子。参数如良好的选择性,效率,更好的疗效与制药动力学工具。然而,大多数的先导化合物经过结构修饰以满足其特定的生物学特性,即所谓的先导优化。然而,所研究的先导化合物必须满足五个特征,才能作为具有生物活性的药物分子。它们是效价、持续时间、安全性、可用性和药物可接受性,其中效价涉及任何分子在较小数量下表现出理想药物特性的能力。生物利用度标志着药物化合物经过多重屏障到达目标部位的运输称为生物利用度。持续时间的概念标志着药物分子及其药理反应进入的时间。安全规则涉及毒性参数,这些毒性参数显示对目标生物体的副作用较少或无副作用。因此,上述所有因素对药物分子的先导优化都有同样的贡献。快速发现药物的目的包括靶点识别和验证。 Upon target validation process, identification of hits and lead discovery phases has to be developed for a novel drug discovery process. Although, physical and biochemical parameters were used to decide the change in the structural property of the compounds to synthesize an effective lead molecule for the development of the drug. Several natural leads have become available in various databases and the literature with biological activity against its specific target, which leads to chemical modification. They fall into 3 categories such as natural, synthetic, and semi-synthetic.
领导优化及其策略
任何先导化合物都可以在结构上进行修饰,并保持其理化性质、热力学、药代动力学参数和毒性(Jogensen, 2009)。根据利平斯基的五键规则,药物必须遵循一些特征,如少于5个氢键和少于10个受体键。分子质量应小于500Da,其分配系数(p- log)不应大于5(Lipinsk et al., 2003)。引线的优化只依赖于结合参数,这些参数显示了有关药物疗效和发生在生物体中的代谢过程的信息。有机合成化学的分支包括结构的简化、修饰、动力学和动力学参数、官能团的相互转换和键的选择性/强度。其他参数如动力学包括热力学,药效学以及ADMET性能的更高改进也必须考虑。
以下是天然产物活性化合物及其应用列表
| 年代。N。 | 天然化合物 | 活性类似物 | 应用程序 |
| 1. | 吗啉 | 布托啡诺、镇痛新、美沙酮 | 靶向阿片受体激动剂和拮抗剂 |
| 2. | 下 | Eribulin,甲磺酸 | 抗肿瘤活性 |
| 3. | Myriocin | Fingolimod | 免疫抑制剂 |
| 4. | Trichostatin一 | Vorinstat | 组蛋白脱乙酰酶抑制剂 |
| 5. | Schisandin C | 双环醇 | 抗乙型肝炎活性 |
| 6. | Asperlicin | Devazepide | 缩胆囊素受体拮抗剂。 |
药物设计的最新趋势
药物的重新用途(药物重新定位、重新配置或重新定位)是一种确定所有超出实际医学指征或试验药物的潜在应用的方法(Ashburn & Thor, 2004)。这一概念可称为药物再分析,即发现已批准/失败/废弃化合物的新适应症,用于治疗不同疾病。
结论
CADD作为现代药物开发的多学科方法发挥作用。其中一个主要的挑战是开发出一种非常适合患者并具有更好疗效的药物。CADD方法已经变得更加精确和有效。在相似搜索平台的化合物搜索、靶点识别、结构预测、结合位点活性预测/验证、生理条件下蛋白质-蛋白质相互作用的知识、ADMET性质的计算、使用QSAR等工具的生物活性估计方面有了显著的改进,以上都指导了引物的必要变化,以提高疗效和选择性。现有的现代药物发现意味着基因组学、生物信息学、计算化学和虚拟筛选的组合化学、HTS、联想配体的知识。然而,LBDD的概念主要依赖于药物规划,即通过试验和错误方法开发一个简单的药物分子,一个3D,提高化合物的整体生物活性。本文介绍了配体药物设计的一些软件和基本原理。
计算机辅助药物设计(CADD)的应用
CADD的研究背景主要基于以下三个方面:1)根据目标结构筛选大量分子,并通过计算和实验对目标结构进行评估;2)根据先导化合物的亲和性、药代动力学参数和毒性指导先导化合物的优化;3)根据结构设计新化合物,以提高其作为药物化合物的功能。CADD用于药物建模的适用性考虑了组合化学和生物信息学,这解决了包括成本和时间持续时间在内的主要问题。
的局限性计算机辅助药物设计(CADD)
虽然SBDD方法已被证明是药物设计的先驱,但它必须跨越社区必须看到的挑战。这种增强包括筛选方法、化学基因组化合物、数据改进、各种工具和数据库的数量和质量、修改多靶点药物结构、毒性预测算法、整合方法以获得更好的疗效和兼容性。另一个最容易探测到的参数是静电相互作用,熵计算被完全忽略。最重要的是,目前还没有一种软件或软件包可以很好地适用于特定的靶标和配体(包括水分子),而且可能的靶标确认和其他创新仍然需要解决。
参考文献
- Suchitra M. Ajjarapu, Apoorv Tiwari, Pramod Wasudeo Ramteke, Dev Bukhsh Singh, Sundip Kumar,第15章-基于配体的药物设计,Dev Bukhsh Singh, Rajesh Kumar Pathak编辑,生物信息学,文献出版社,2022年,233-252页。
- 杨SY。药物发现中的药效团建模与应用:挑战与最新进展。《今日药物发现》2010年6月15(11-12):444-50。doi: 10.1016 / j.drudis.2010.03.013。Epub 2010年4月1日PMID: 20362693。
- 约根森王。高效的药物先导发现和优化。Acc化学物.2009年,42(6):724 - 733。doi: 10.1021 / ar800236t
- 士兵马克里尼察,利库拉斯,m.s,斯派鲁里亚斯,G.A.和m.t马苏卡斯。(2018)。在网上药物设计。在eLS, John Wiley & Sons, Ltd (Ed.)。https://doi.org/10.1002/9780470015902.a0028112
- 吕伟,张锐,蒋辉,张辉,罗聪。表观遗传学中的计算机辅助药物设计。前化学.2018; 6:57。2018年3月12日发布。doi: 10.3389 / fchem.2018.00057。

