表的内容
通常,细菌细胞由细胞壁,细胞膜和细胞核组成。细胞壁是含细菌的肽聚糖层的外覆盖物,其由交联聚合物组成。肽聚糖主要负责所有包括电阻率的机制,毒力因子,包括细菌的形状。
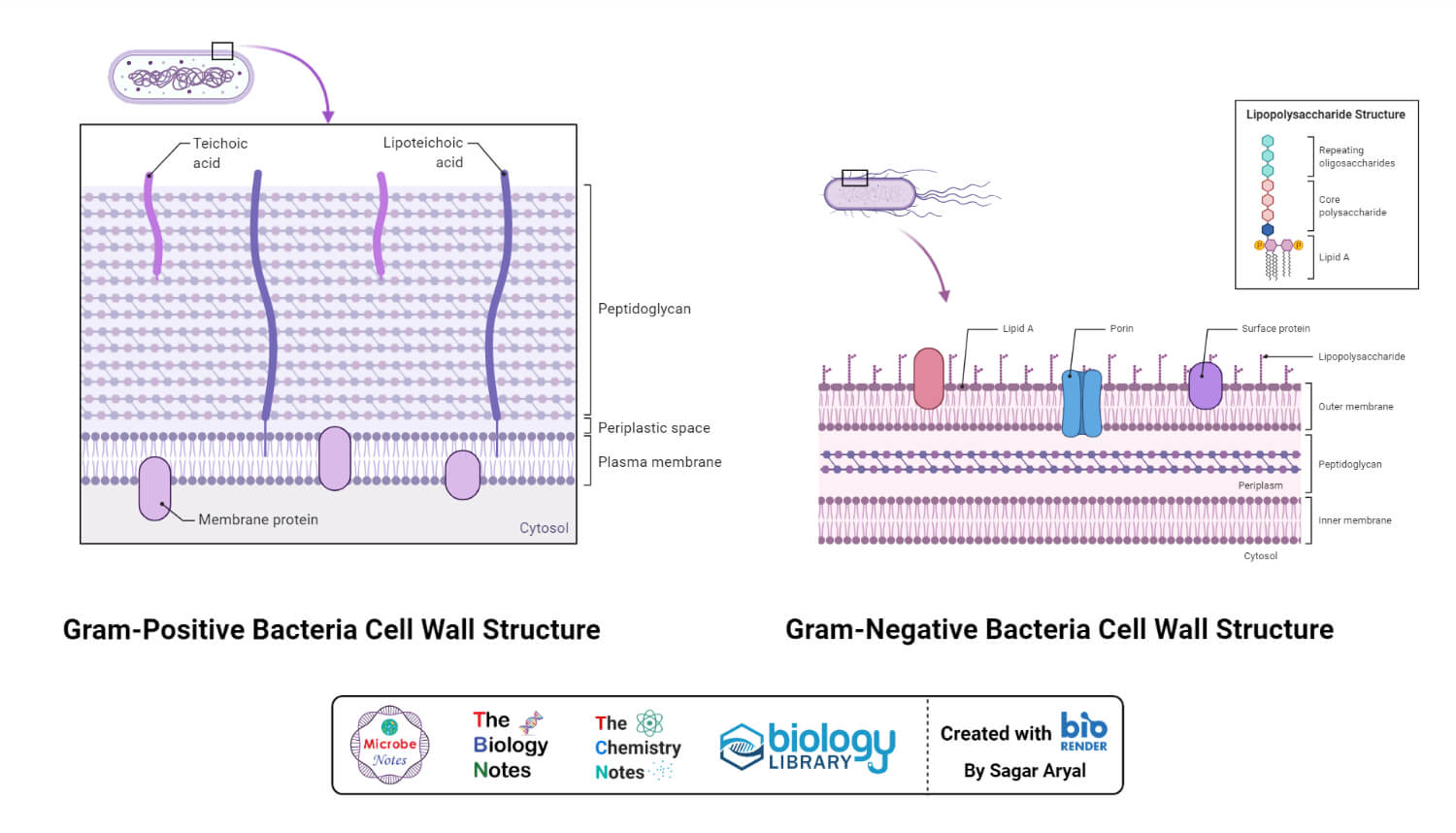
什么是细胞壁合成抑制剂?
细胞壁合成抑制剂包括β-内酰胺类和糖肽的抗生素。β-内酰胺抗生素由青霉素,头孢菌素,单食用菌和碳癌蛋白组成。糖肽包括万古霉素和Teicoplanin,这是该类最常用的抗生素。青霉素包括氨苄青霉素,牛奶蛋白,头孢菌素包括头孢哌酮,头孢噻肟,单食药包括阿兹特瓜,这是该类唯一可商购的抗微生物剂。Carbapenem由Imipenem,Meropenem和Ertapenem组成。细胞壁合成抑制剂是用于治疗的最常用的抗生素克消极也革兰氏阳性感染。
表:细胞壁生物合成抑制剂及其目标。表源:https://doi.org/10.1039/c6md00585c
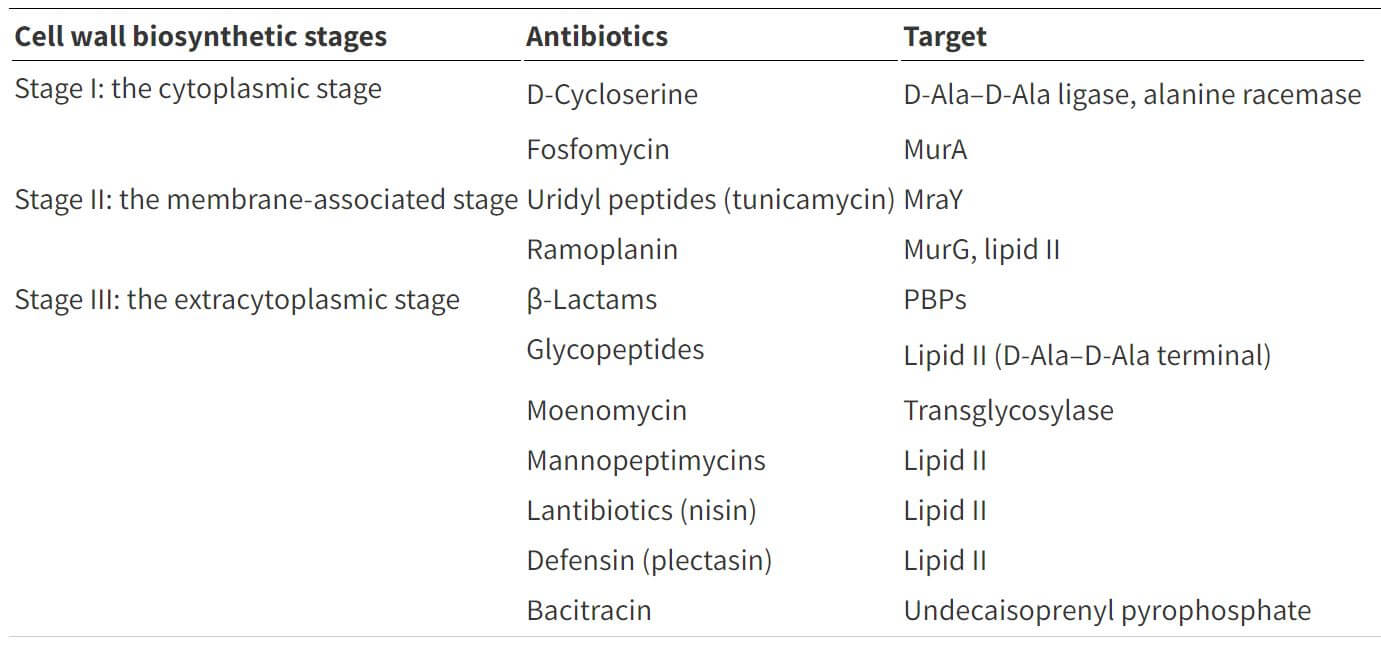
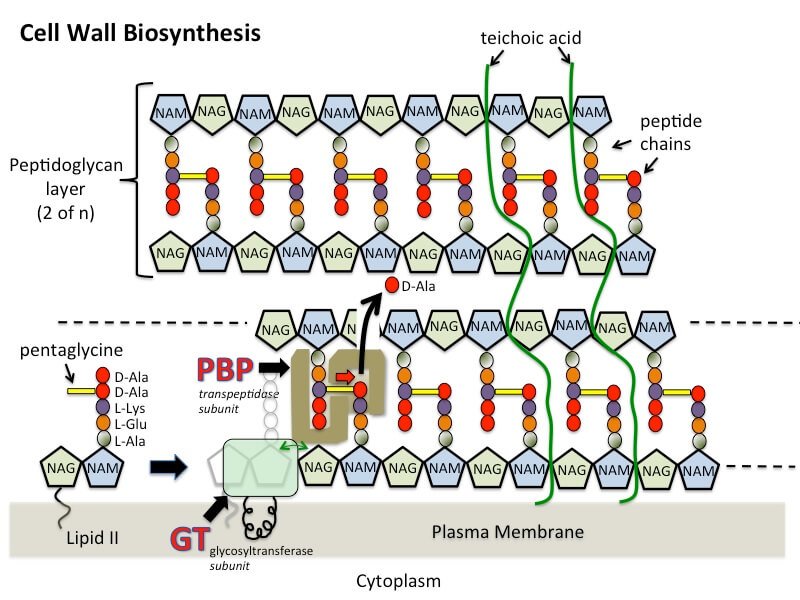
- 肽聚糖由肽和聚糖的聚合物组成。主要是肽聚糖的合成在三个阶段中发生;细胞质,膜和周质。
- 在细胞质阶段,UDP-GlcNAc在四个步骤过程中催化。穆拉和麦格催化形成UDP-Murnac。四种酶MUR C,MUR D,MUR E和MUR F催化丙氨酸,谷氨酸涉及重要步骤。丙氨酸连接酶和丙氨酸外周期是参与D-Ala-D-Ala的形成的两个重要酶。
- 第二膜相关阶段包括形成脂质中间体。
- 在第三阶段,通过糖基转移酶形成肽聚糖链,然后通过酶转发酶交联。该酶转琥珀肽酶由PBPS(青霉素结合蛋白)和棒A组成
- MUR酶,转发酶,糖基酶和脂质组分是涉及细胞壁合成的主要成分。
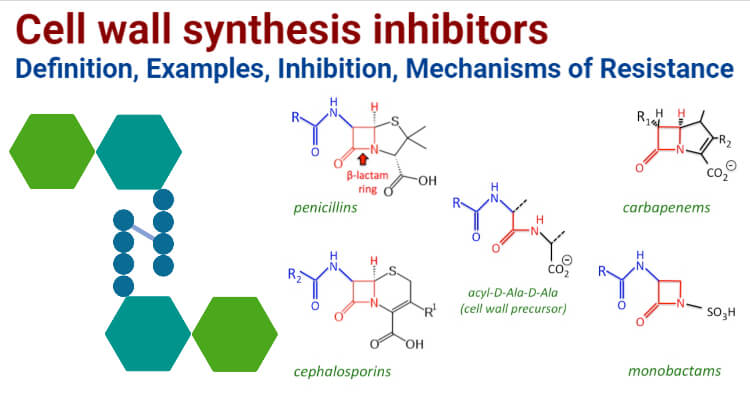
细胞壁合成抑制剂的实例
β-内酰胺抗生素
a .青霉素-氨苄西林,阿莫西林,哌拉西林,苯唑西林
头孢菌素:
- 第一代:Cefazolin,Cefalexin
- 第二代:Cefoxitin,头孢呋辛
- 第三代:Cefixime,Ceftazidime,Ceftriaxione
- 第四代:头脑
c。Monobactams:阿兹曲那姆,市面上唯一一种单巴坦。
d。碳青霉烯:Imipenem,Meropenem.
糖肽
万古霉素,oritavancin,teicoplanin,telavancin,blleomycin,ramoplanin,decaplanin。
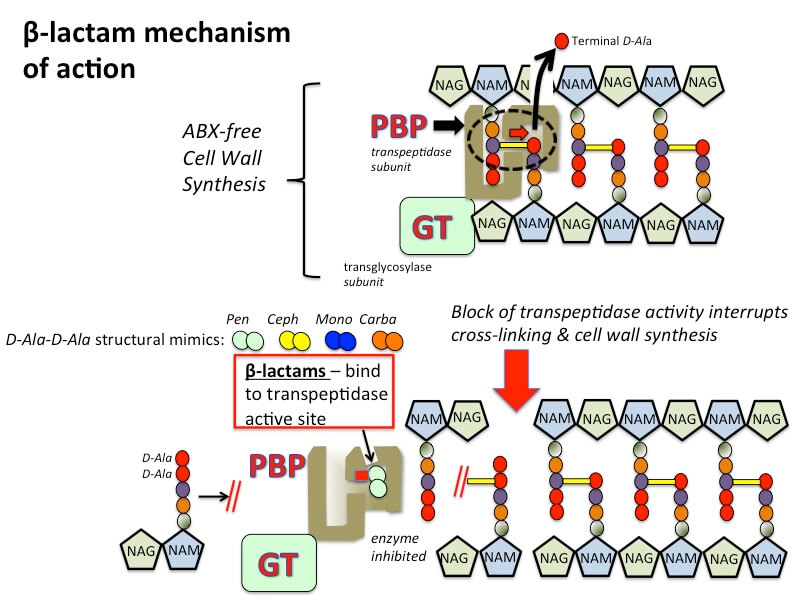
抑制的过程/步骤
- β-内酰胺通过用作二肽酶反应中的转酯酶酶的用作D-丙氨酸-D-丙氨酸的组分干扰合成。甘氨酸残留在青霉素结合蛋白(PBPS)存在下肽链的交联氨基酸部分。形成新的肽聚糖链,导致细胞破裂引起的渗透裂解。
- 细菌细胞含有自溶酶,这是已知的细胞生长和分裂和β -内酰胺抗生素影响自溶活性,导致细菌细胞死亡。
- 糖肽抗生素结合脂质II组分,防止中央脂质转运蛋白在作用模式中起到重要作用的中枢性脂质转运蛋白。它们通过与五肽链连接并防止添加新的肽聚糖单元来抑制肽聚糖合成。通过这种相互作用抑制胰糖基化和转蛋白导致细菌细胞死亡。
- 万古霉素,糖肽的最后一个手段药物可防止D-丙氨酸与青霉素结合蛋白的结合,该蛋白质抑制细胞壁合成引起细菌裂解。
- 细菌细胞膜的透氧和去极化导致一些糖肽的细胞壁合成抑制。
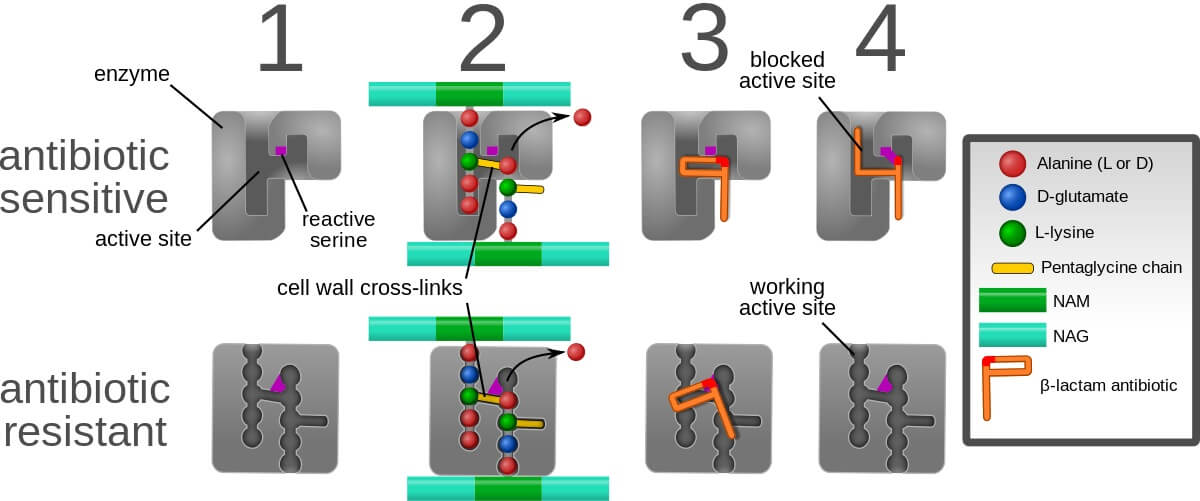
抵抗机制
药物的亲和力,其渗透性和稳定性决定了对细菌的活性。在过去的二十年中,对抗生素的抗性有机体增加了很大的关注。生物通过合成PBP2A(青霉素结合蛋白2a),对β-内酰胺抗生素产生抗性。它具有低亲和力,允许经肽酶活性,这导致患者的细菌殖民化。染色体突变也直接或间接地增加青霉素结合蛋白2a和转录的水平导致细菌抗性。β-内酰胺抗性主要是由于青霉素结合蛋白和酶促降解的改变。糖肽电阻率是由于靶的改变。
- 革兰氏阳性菌和革兰氏阴性菌都产生β -内酰胺酶。在革兰氏阳性菌中,青霉素酶是引起对抗生素耐药性的酶,也可以通过改变酶的活性引起突变。
- 革兰氏阴性生物可以表达染色体以及质粒介导的酶,所述质粒介导的酶在引起电阻率方面具有广泛的活性。
- 耐甲氧西林和苯唑西林S.金黄色葡萄球菌含有MEC A基因的金葡萄球菌染色组MEC。PBP2A由MEC进行编码,该基因显示出高抗β-内酰胺抗生素的基因。
- 不同的抗生素通过膜蛋白质从细胞出口,以保持其浓度,称为Efflux泵。这些泵带来了各种抗生素,有助于形成MDR生物。
- d -丙氨酸转化为d -丙氨酸乳酸,抑制糖肽的交联从而产生抗性。
- 七个范基因负责导致万古霉素抗性。这些基因编码脱氢酶,其形成乳液,这对于形成未改性的肽聚糖是重要的。
- 转移质粒转移所需的不同酶的表征导致万古霉素抗性。
参考文献
- Canzani D和Aldeek, F.(2017)。青霉素G的功能、代谢物、过敏和耐药性。1(1)。
- Ghooi,R. B和Services SC。(2018)。抑制细胞壁合成 - 这是青霉素作用的机制?9877(4月),2-7。https://doi.org/10.1016/0306-9877(95)90085-3
- 康H和Park Y(2015)。糖肽抗生素:结构和作用机制。45(2),67-78。
- Kapoor G,Saigal S和Elongavan A(2017)。抗生素的动作和抗性机制:临床医生指南。麻醉学与临床药理学杂志。33:300-305
- Nikolaidis I和Dessen A(2014)。针对细菌细胞壁的抗生素耐药性。23日,243 - 259。https://doi.org/10.1002/pro.2414
- Scheffers,D和Pinho M G.(2005)。细菌细胞壁综合:本地化研究的新见解。69(4)。585-607。https://doi.org/10.1128/mmbr.69.4.585
- Singh M,Chang J,Coffman L,Kim S J和美国U.(2018)。HHS Public Acces.S.。121(16),3925-3932。https://doi.org/10.1021/acs.jpcb.7b00324.a.
来源
- https://www.researchgate.net/publication/268793620_multidrug_efflux_pumps_in_gramnnegative_
bacteria_and_their_role_in_antibiotic_resistance - 6% - https://www.sciencedirect.com/topics/neuroscience/peptidoglycan- 4%
- https://www.sciencedirect.com/topics/immunology-和--microbiology/peptiDoglycan- 3%
- https://www.sciencearect.com/topics/biochemisty-genetics-and-molecular-biology/peptidoglycan- 2%
- https://www.sciencedirect.com/science/article/abs/pii/S0045206814000224- 1%
- https://globalrph.com/infectious-disease-list/monobactams/- 1%
- https://pubs.acs.org/doi/10.1021/acs.jpcb.7b00324- 1%
- https://pubs.asahq.org/aneshesiology/article/129/2/335/17980/presumed-lactam-allergy-和--AncrossRestivity-
in-1% - https://docs.ufpr.br/~microgeral/regulacaopeptideoglicana.pdf-1%

