表的内容
莱姆病的发病机理由Borrelia Burgdorferi.
- 莱姆病是由螺旋体引起的b . burgdorferi,是由该属的小蜱虫叮咬传播的Ixodes.。
- 人类是“偶然”的宿主B.Burgdorferi.因为受感染者的螺旋体不会传染给其他宿主。
- 在里面的中间Ixodes.在喂食期间,蜱虫的螺旋体B.Burgdorferi.处于附着于上皮细胞的休眠,非复制状态。
- 它们表达了一种质粒编码的主要外表面蛋白(OSPA.),在保护方面发挥着关键作用B.Burgdorferi.来自免疫宿主的血液中存在的抗体,并且还可以通过结合蜱胚胎细胞受体来促进蜱胚胎定子。
- 外表面蛋白A(OSPA)在表面上表示B.Burgdorferi.居住在未凝固的蜱的中间肠道中,并与肠道蛋白特别结合。
- 在进料时,将该蛋白质的表达被抑制,使螺旋体迁移到唾液腺,并且外表蛋白C(OSPC)表达,这对于从蜱传播到哺乳动物的传播至关重要。
- 在人类中,被感染的蜱虫的叮咬是通过健康皮肤引入病原体的必要条件。
- 这种细胞外病原体开始于真皮组织,在那里它开始通过改变其表面糖蛋白的表达来适应哺乳动物宿主的生活。
- 螺旋体的基因表达分布响应于滴定送料的变化,由OSP到OSPC的切换为必要的。
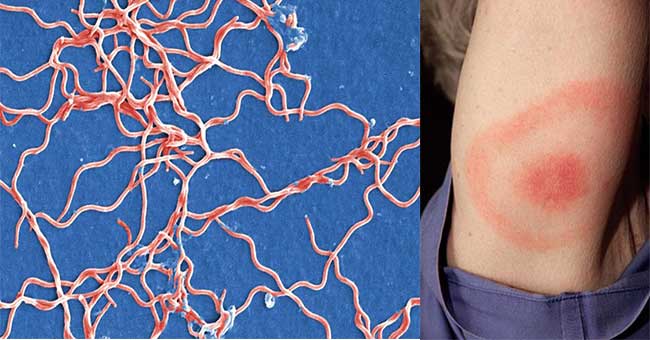
- 能力B.Burgdorferi.在哺乳动物宿主的皮肤上繁殖和建立感染是反映在哺乳动物宿主皮肤上的特征体征之一局部感染或第1阶段人类的莱姆病,红斑迁移(EM)皮疹,反映淋巴细胞和巨噬细胞的浸润。
- 螺旋体是高丝动力,可能涂有宿主蛋白酶纤溶酶。
- 经过一定的时期,它们能够传播通过皮肤,导致皮疹的扩张,留下烫伤的中央区域,以及靶心的外观。
- b . burgdorferi表达通过与整联蛋白,糖胺聚糖,纤维连接蛋白和胶原的特异性相互作用,表达与内皮细胞,血小板,软骨细胞和细胞外基质的外表面蛋白质。
- 这些相互作用对包括皮肤、关节和心脏在内的组织的归巢和定植非常重要,细菌也激活蛋白酶和其他诱导的宿主细胞分子,允许通过血液传播到其他组织。
- 弥散性感染(第二阶段)包括短暂的血流定植。
- 在这种阶段,在多个地点中可以看到一定程度的血管损伤,包括温和的血管炎或血管性血管闭塞,表明螺旋螺旋化血管堵塞。这个阶段被称为早期播种感染或第二阶段莱姆病。
- 之后,在后期阶段或第三阶段莱姆病时,细菌的增殖率明显降低或被宿主防御系统控制,导致组织中细菌的数量非常低。
- 主机响应b . burgdorferi在疾病发病机制中起关键作用。
- b . burgdorferi不产生毒素或蛋白酶,对定植后的组织损伤直接负责。
- 相反,细菌产生了多种激活宿主反应的多个分子,并且可以导致局部化和广义炎性致病反应。
- 大多数这些宿主反应通常用于含有或清除感染,并且是先天防御和/或炎症反应的组成部分。
- 然而,这些细菌并不能被宿主免疫反应消灭。
- 一旦人类感染,尽管宿主产生了强烈的免疫反应,但螺旋体可以存活数年。
- b . burgdorferi能够结合哺乳动物补体调节因子,这可能在宿主组织的持续感染期间提供对补体介导的裂解和调理剂的抵抗力。
临床表现Borrelia Burgdorferi.
莱姆病
- 莱姆病分为三个阶段。
- 第一阶段,红斑迁移(EM),是具有中央清洁的特征红色,环形皮肤病变,首先出现在蜱咬的遗址,但也可能在远处发展。
- 临床表现包括头痛,发烧,肌肉和关节疼痛,在此阶段的萎靡不振。
- 第二阶段,可能包括关节炎,但最重要的特征是神经系统疾病,包括脑膜炎,神经系统缺陷和心脏炎。
- 这是对器官和组织的螺旋形化的血液源性传播的结果。
- 此外,脑膜,脊髓,周围神经和脑中可能发生神经系统症状和感染。
- 第三阶段通常表现为慢性关节炎或慢性萎缩性肢端皮炎(ACA),一种弥漫性皮疹,并可持续数年。


写得很好,外行也能理解。我有你们所说的第三阶段,有人叫它:治疗后莱姆病综合症,慢性莱姆病,或者,世界著名的:“没有慢性莱姆病这种东西。”谢谢你做研究,传播消息。